Si sente parlare molto spesso dell’ insulina. Sembra che tutti (o comunque tutti quelli interessati all’argomento) considerino questo ormone come nemico numero uno della buona alimentazione, e lo colleghino all’uso di carboidrati ad alto indice glicemico (pochi parlano di alto carico glicemico): pane, pasta, riso e patate.
Cerchiamo di mettere un pò più a fuoco l’argomento.
Cos’è l’insulina?

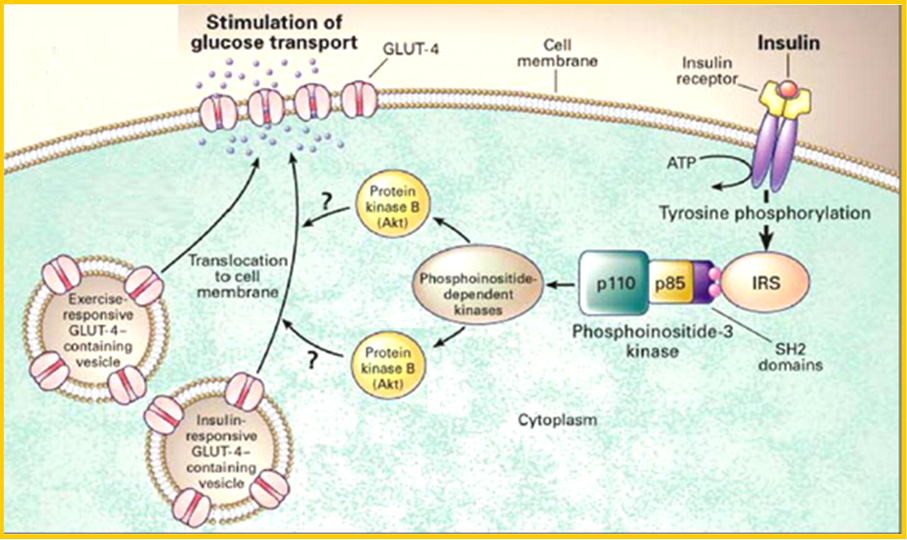
Legame insulina-recettore
L’insulina è un ormone peptidico, prodotto dalle cellule beta delle Isole di Langerhans, del pancreas. E’ formata da due catene: catena A di 21 aminoacidi e catena B di 30 aminoacidi, unite da due ponti solfuro. La sua funzione principale è quella di stimolare la fase sintetica del metabolismo: infatti, promuove l’assunzione di glucosio da parte delle cellule dei tessuti periferici, di aminoacidi e stimola la sintesi del glicogeno, dei trigliceridi, di colesterolo e degli aminoacidi. Quindi, ha azione sui glucidi, grassi e proteine:
Glucidi:
- stimola l’utilizzazione del glucosio facilitandone il passaggio dal sangue alle cellule
- stimola la glicogenosintesi
- inibisce la glicogenolisi
Lipidi:
- promuove il passaggio degli acidi grassi dal sangue alle cellule
- stimola la lipogenesi e l’esterificazione degli acidi grassi in trigliceridi
- inibisce la lipolisi
- stimola la sintesi di colesterolo
Proteine:
- promuove il passaggio degli amminoacidi dal sangue alle cellule
- stimola la sintesi delle proteine
- inibisce la gluconeogenesi
L’insulina delocalizza il glucosio ematico
Il glucosio non ha la capacità di entrare liberamente nelle cellule. L’insulina, stimolando l’utilizzazione del glucosio, ne regola i livelli ematici, cioè la glicemia:
quando la glicemia si alza, aumenta la secrezione di insulina dalle cellule del pancreas.
Nel muscolo scheletrico, nel cuore e nel tessuto adiposo bianco e bruno, il principale trasportatore di glucosio è il GLUT-4. Questi tessuti sono definiti insulino-dipendenti.
Un altro trasportatore particolare di glucosio è il GLUT-2 che è espresso soprattutto a livello epatico e nel pancreas: questo trasportatore è di tipo bidirezionale, quindi capace di lavorare in entrambe le direzioni, dalla cellula verso il liquido interstiziale e viceversa. Questa funzione è molto importante poichè nel fegato avviene la gluconeogenesi, cioè la formazione di glucosio a partire soprattutto dagli aminoacidi, che quindi viene captato all’interno, ma anche espulso nel sangue per riportare la glicemia alla stabilità.
Nel cervello e nei globuli rossi, invece, sono espressi trasportatori di glucosio insulino-indipendenti, come il GLUT-1, il cui livello aumenta al diminuire della glicemia, e sono capaci di captare glucosio anche quando il suo livello è estremamente basso.
L’ormone dell’accumulo
Da come si evince, grossolanamente potremmo definirlo l’ormone dell’accumulo, in quanto se è essere stimolato crea le condizioni metaboliche per la sintesi.
Ciò non significa assolutamente che deve essere inibito, in quanto è un ormone di vitale importanza per la vita. Ma deve lavorare entro un range, una “zona“, e ciò può accadere se scegliamo la qualità e poi anche la quantità di alimenti da assumere quotidianamente, che ci portano all’obiettivo da raggiungere: utilizzare cioè il cibo come strategia per controllare gli ormoni.
Quando stimoliamo troppo l’insulina
Quando mangiamo troppi carboidrati ad alto carico glicemico, i livelli di glucosio ematico (glicemia) salgono rapidamente. Poichè elevate concentrazioni di glucosio sono tossiche, l’organismo reagisce secernendo insulina per delocalizzare l’eccesso in cellule adipose, muscoli, e fegato. Se la glicemia si alza troppo rapidamente, si ha un’eccessiva produzione di insulina e i livelli di glucosio ematico si abbassano altrettanto rapidamente, con conseguente ipoglicemia: così due ore dopo un bel piatto di pasta stentiamo a tenere gli occhi aperti e siamo affaticati. Se questo lo si fa tutti i giorni, le cellule, “spaventate” dalle ondate massicce di insulina che vengono secrete, nascondono i recettori esposti sulla loro superficie, (come se scattasse un meccanismo di difesa per la salvaguardia della loro vita): così il glucosio circolante non viene delocalizzato bene, resta in circolo, e paradossalmente l’organismo che fa? Fa secernere ancora più insulina dal pancreas per delocalizzare quel glucosio, innescando un meccanismo perverso in cui alti livelli di insulina (iperinsulinismo) alimentano la resistenza delle cellule ad essa (insulino-resistenza). Questo disordine nella trasmissione dei segnali dall’esterno all’interno delle nostre cellule ci fa infiammare, ingrassare, ammalare.

Traslocazione dei recettori dell’insulina dalla membrana cellulare all’interno della cellula in seguito ad una esposizione prolungata delle cellule all’insulina
Quando stimoliamo poco l’insulina
Quando invece non mangiamo abbastanza carboidrati ogni giorno, in qualche modo l’organismo si organizza per far arrivare glucosio al cervello e al resto del corpo: secerne più cortisolo dalle ghiandole surrenali, per cominciare a staccare pezzi di muscoli in modo da formare glucosio da essi, attraverso un processo denominato neoglucogenesi (o gluconeogenesi). Se questo lo si fa ogni giorno, con valori di insulina bassissimi si attivano enzimi (trigliceride-lipasi) che provocano il destoccaggio dei trigliceridi in acidi grassi, che si ritrovano nel sangue a tale concentrazione da essere utilizzati in maniera preferenziale rispetto ai carboidrati: questo utilizzo elettivo dei grassi permette la formazione di corpi chetonici che vengono utilizzati al posto del glucosio, e crea l’acidosi metabolica. Alti livelli di cortisolo causano un treno metabolico di non poco conto: analogamente agli alti livelli di insulina, provocano attacchi di fame continui (dovuti all’insulino-resistenza); maggiore suscettibilità alle infezioni (per via della funzione immunitaria depressa); minore lucidità mentale (per la distruzione dei neuroni dell’ippocampo, per la continua esposizione tossica del cortisolo).
L’insulina e l’infiammazione
L’insulina gioca un ruolo chiave anche nel metabolismo degli acidi grassi essenziali (omega-3, omega-6 ): quando c’è troppo enzima in circolo, infatti, la conversione degli acidi grassi omega-6 della dieta, che ci arrivano soprattutto sottoforma di acido linoleico (gli oli di semi ne sono fonte eccellente) viene dirottata verso la sintesi di acido arachidonico, un acido grasso omega-6 che viene utilizzato dalle nostre cellule per produrre eicosanoidi cattivi (proinfiammatori). L’insulina, difatti, stimola le desaturasi, enzimi chiave nella cascata degli eicosanoidi: più eicosanoidi cattivi produciamo, più produciamo aggregazione piastrinica, aumentiamo la vasocostrizione, cambiamo la permeabilità vascolare e più acceleriamo l’infiammazione cellulare. Tra le conseguenze dell’infiammazione cellulare c’è lo sviluppo stesso dell’insulino-resistenza: gli alti livelli di insulina durante tutto il giorno accelerano la produzione di eicosanoidi infiammatori. (Vedi: infiammazione silente) Ciò crea cambiamenti di omeostasi nelle cellule, e un disturbo nei segnali cellulari: la cellula non risponde più efficientemente agli stimoli, col risultato che crea l’anticamera infiammatoria che proietta alla sindrome metabolica, al diabete e all’obesità.
Tre esempi lampanti che ci portano alla conclusione che non esiste un equilibrio vitale senza una regolazione ottimale dell’ormone in oggetto, che ci possa garantire le basi per il controllo dell’infiammazione cellulare e dell’efficienza metabolica: la capacità, cioè, di trasformare le calorie degli alimenti in energia chimica.
Come? Usando bene il cibo
Molto semplice il discorso ma contestualmente molto complesso. Dalla scelta qualitativa sopratutto, ma anche quantitativa, dei carboidrati della nostra dieta quotidiana, inserita in un quadro alimentare completo, che non trascuri il quantitativo proteico e neanche i grassi (troppo spesso condannati erroneamente), e che assicuri sostentamento energetico con la minima assunzione calorica, si può arrivare a regolare questo ormone chiave del nostro metabolismo, il cui controllo ci può regalare le basi della longevità, e la cui mancanza di controllo ci proietta alle malattie.
Il cibo, una volta introdotto e assimilato nel nostro organismo, scatena una serie di eventi biochimici e risposte ormonali che possono essere anche centinaia di volte più potenti di qualsiasi farmaco! Da questa consapevolezza nasce la possibilità di approcciarsi alla quotidiana alimentazione in modo diverso, concependola come uno strumento per modulare, con l’esercizio costante a tavola – ma che poi diventa un’abitudine come un’altra – il nostro benessere fisico e mentale.
Bibliografia
- General aspects of muscle glucose uptake. Alvim RO, Cheuhen MR, Machado SR, Sousa AG, Santos PC
- Regulation of glucose transporter translocation in health and diabetes. Bogan JS.
- GLUT4 is sorted to vesicles whose accumulation beneath and insertion into the plasma membrane are differentially regulated by insulin and selectively affected by insulin resistance. Xiong W, Jordens I, Gonzalez E, McGraw TE.
-
[Regulation of insulin sensitivity by subcellular GLUT4 targeting]. Shibata H. Rinsho Byori. 2005 Oct;53(10):942-9. Review. Japanese.
-
Insulin receptor substrates-1 and -2 are both depleted but via different mechanisms after down-regulation of glucose transport in rat adipocytes. Renström F, Burén J, Eriksson JW. Endocrinology. 2005 Jul;146(7):3044-51. Epub 2005 Apr 21.
-
Lipid signals and insulin resistance. Zhang C, Klett EL, Coleman RA. Clin Lipidol. 2013 Dec;8(6):659-667.
-
Desaturase activities and metabolic control in type 2 diabetes. Sartore G, Lapolla A, Reitano R, Zambon S, Romanato G, Marin R, Cosma C, Manzato E, Fedele D. Prostaglandins Leukot Essent Fatty Acids. 2008 Jul-Aug;79(1-2):55-8. doi: 10.1016/j.plefa.2008.07.001. Epub 2008 Sep 3.
-
Mechanism linking diabetes mellitus and obesity. Al-Goblan AS, Al-Alfi MA, Khan MZ. Diabetes Metab Syndr Obes. 2014 Dec 4;7:587-91. doi: 10.2147/DMSO.S67400. eCollection 2014. Review.
-
Associations Among Fatty Acids, Desaturase and Elongase, and Insulin Resistance in Children. Beccarelli LM, Scherr RE, Newman JW, Borkowska AG, Gray IJ, Linnell JD, Keen CL, Young HM.J Am Coll Nutr. 2018 Jan;37(1):44-50. doi: 10.1080/07315724.2017.1347908. Epub 2017 Oct 18.
-
Omega-6 polyunsaturated fatty acids, serum zinc, delta-5- and delta-6-desaturase activities and incident metabolic syndrome. Yary T, Voutilainen S, Tuomainen TP, Ruusunen A, Nurmi T, Virtanen JK. J Hum Nutr Diet. 2017 Aug;30(4):506-514. doi: 10.1111/jhn.12437. Epub 2016 Nov 7.